생명과학 II(9)
세포는 다양한 물질로 구성되며, 이러한 물질에는 유기분자, 무기분자, 이온 등이 있다. 본문에서는 그중 단백질에 대해 알아볼 것이다.
단백질(Protein)
단백질은 아미노산의 펩타이드 결합으로 만들어지는 고분자 유기물질이다. 단백질의 단위체는 아미노산이며, 아미노산의 화학식은 \( \mathrm{N} \mathrm{H}_{2} \mathrm{C} \mathrm{H} \mathrm{R}_{n} \mathrm{COOH} \)이다. 즉, 탄소(\( \mathrm{ C } \)), 수소(\( \mathrm{ H } \)), 산소(\( \mathrm{ O } \)), 질소(\( \mathrm{ N } \))가 주성분이 되는 유기분자이다. 20종 정도의 아미노산이 존재한다.
단백질은 종류에 따라 특이적인 입체 구조를 가지고 있어 생체 내에서 다양한 작용을 한다. 특히 효소, 호르몬, 항체의 주성분이며, 물질대사 및 생리작용을 조절하고 방어 작용에 관여한다. 다만 열이나 산 등에 의해 단백질의 입체 구조가 쉽게 파괴된다. 이를 단백질의 변성이라고 한다. 단백질이 변성되면 본래의 기능을 상실한다. 단백질의 변성에 대해서는 추후 효소를 다루면서 자세히 다루도록 하겠다.
아미노산의 구조

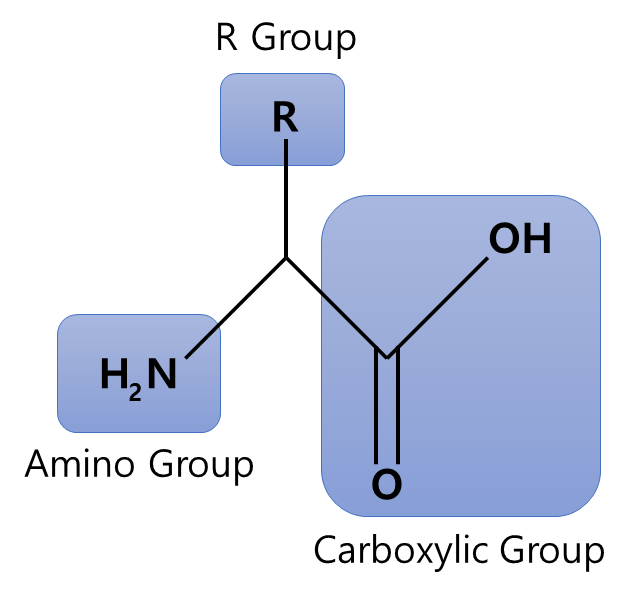
아미노산은 3가지 그룹(기, Group)을 가진다. 중심 탄소에 수소(\( - \mathrm{H} \))와 아미노기(Amino Group), 카르복실기(Carboxylic Group), 곁사슬기(R기, R Group)가 각각 하나씩 결합되어 있는 구조를 가진다. 아미노기는 (\( - \mathrm{N} \mathrm{H}_{2} \)) 꼴로 이루어져 있으며, 이온화하여 (\( - \mathrm{N} \mathrm{H}_{3}^{+} \)) 꼴이 된다. 카르복실기는 (\( - \mathrm{COOH} \)) 꼴로 이루어져 있으며, 이온화하여 (\( - \mathrm{COO}^{-} \)) 꼴이 된다. R기는 (\( - \mathrm{ R } \)) 꼴로 이루어져 있으며, 아미노산 20종에 대응되는 20종의 R기가 존재한다. R기의 구조에 따라 단백질의 구조가 달라지며, 물에서의 용해도 및 이온화도, 이온 상태의 아미노산의 전하 등 다양한 물리 화학적 특성을 결정한다.
아미노산의 펩타이드 결합(Peptide Bond)

펩타이드 결합은 두 아미노산 간에 일어나는 동화작용이다. 이러한 펩타이드 결합을 통해 아미노산 서열이 신장되며 단백질을 이룬다. 펩타이드 결합이 일어나면 한 아미노산의 카르복실기와 다른 아미노산의 아미노기가 떨어지면서 결합한다. 이때, 카르복실기에서는 (\( - \mathrm{OH} \))기가, 아미노기에서는 (\( - \mathrm{H} \))가 각각 하나씩 떨어져 나가며 물(\( \mathrm{H}_{2} \mathrm{O} \))을 생성한다. 펩타이드 결합은 물을 생성하며 결합하는 반응이므로 탈수 축합 반응의 한 종류이다.
생명체와 무생명체 간에 기본적인 차이점이란 없다.
물질의 진화과정에서 생명을 특정 짓는 요소와 생명체의 발현이라는 복잡한 결합이 틀림없이 일어날 수 있었을 것이다.
-오파린